Die Zahl der Tweets des Ministers, in denen er sich auf Studien beruft, die Eric Topol für ihn gelesen hat, ist Legion. Dieser fehlt:
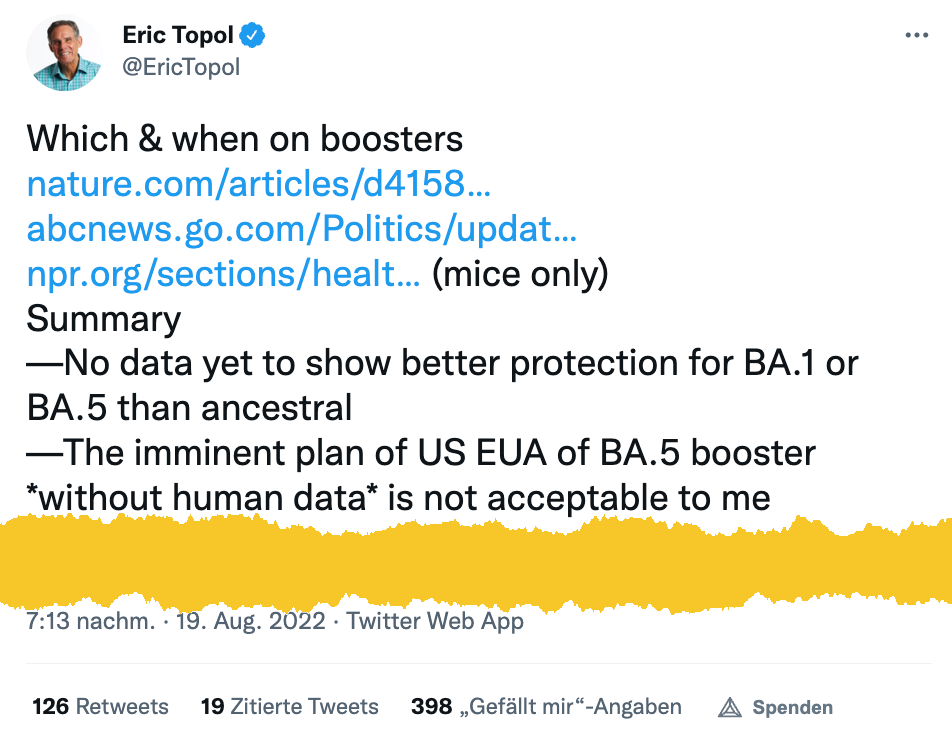
Topol bezieht sich auf das US-Zulassungsverfahren, das ohne klinische Studien arbeitet (Corona ist halt ein Notfall, da braucht es Notfallzulassungen). Doch genau das ist auch in Europa geplant. Hier wird als Begründung angeführt, auch für die Grippeimpfungen bräuchte es keine neuen Studien, außerdem gebe es hier keine Notfallzulassungen. In der Tat nennen sie sich bedingte Zulassungen, die aber gleichermaßen auf ausführliche Studien vor der Genehmigung verzichten.
Topol dazu:

Aufmerksam auf diesen Thread wurde ich durch einen Tweet vom 22.8. mit der Frage "@Sander_Lab, @Karl_Lauterbach, warum haben Sie diesen Tweet von @EricTopol denn nicht verlinkt?".
Siehe dazu auch:

Daten haben die noch nie gebraucht. Es genügen Behauptungen. Hat doch bestens funktioniert bis jetzt.
Dieser Beitrag auf tkp legt nahe, dass mehr als drei Injektionen kontraproduktiv bis ziemlich gefährlich sein können. Leider reicht meine Fachkenntnis an dieser Stelle nicht aus, das zu beurteilen, es geht da schon etwas ins Detail, aber vielleicht mag sich ja jemand Bewanderter aus dem Leserkreis dazu äußern?
https://tkp.at/2022/08/23/studie-mehrfache-mrna-dosen-machen-krank-durch-igg4-antikoerper/
Es handelt sich mal wieder um einen Preprint.
… und es werden weitere nicht zugelassene Stoffe für viele Euro je kg, äh, Impfung bestellt.
"Mediziner warnen vor Tomaten-Grippe"
https://m.bild.de/ratgeber/gesundheit/ratgeber/tomaten-grippe-ausbruch-in-indien-81092548.bildMobile.html
Wahrlich, ein integerer Wissenschaftler:
https://nitter.net/pic/orig/media%2FFa2hBx8XgAIBy1G.jpg
@Eddy Salino: Lauterbach hat wahrlich genug Dreck am Stecken. Da muß man ihm nicht "Millionen Menschen" anhängen, die an Lipobay und Reductil gestorben sein sollen.
Siehe auch Karl Lauterbach: Trotz Lipobay-Skandal Berater der Deutschen Regierung – Skandale und Fehlverhalten und
Kanzler und Gesundheitsminister: Rapport in Leverkusen
Ausführlich: "Manchmal haben wir Mist gebaut oder uns dumm angestellt, und wir machen uns keine Illusionen darüber, dass das nicht wieder passieren wird… und wieder." und
https://www.corodok.de/karl-lauterbach/.
Ja, ja, nur nicht über die Stränge schlagen lassen, … da sei der Aschmoneit vor.
Damit es die neuen, angepassten „Impfstoffe“ auch rechtzeitig über die Ziellinie schaffen, wird die EMA am 1. September eine Sondersitzung abhalten.
Extraordinary meeting of the Committee for Medicinal Products for Human Use (CHMP): 1 September 2022
Date: 01/09/2022
Location: Online
This extraordinary meeting is organised to discuss the evaluation of two applications for adapted mRNA COVID-19 vaccines which more closely match the original strain and the BA.1 Omicron subvariant. One application was submitted by Moderna for Spikevax (previously COVID-19 Vaccine Moderna) and one by Pfizer/BioNTech for Comirnaty.
The aim of the meeting is to conclude the evaluation of the two applications, if possible.
The Committee for Medicinal Products for Human Use (CHMP) is responsible for preparing the European Medicines Agency's opinions on all questions concerning human medicines.
https://www.ema.europa.eu/en/events/extraordinary-meeting-committee-medicinal-products-human-use-chmp-1-september-2022
Jetzt wissen wir auch, warum Lauterbach bereits mit einer Zulassung des ersten adaptierten „Impfstoffes“ von BioNTech/Pfizer zum 1. September rechnet. Es ist doch alles nur noch Formsache.