Dieser Titel auf aerzteblatt.de vom 21.11.23 zeigt: Der Stand kann eine erneute Pandemie und entsprechende Vergütungen kaum erwarten. Während WEF und WHO noch mit sozialen Phrasen punkten wollen (s. den vorigen Beitrag), formuliert man hier ungeschminkt im Bericht über das Symposium des Lobbyverbands Paul-Martini-Stiftung:
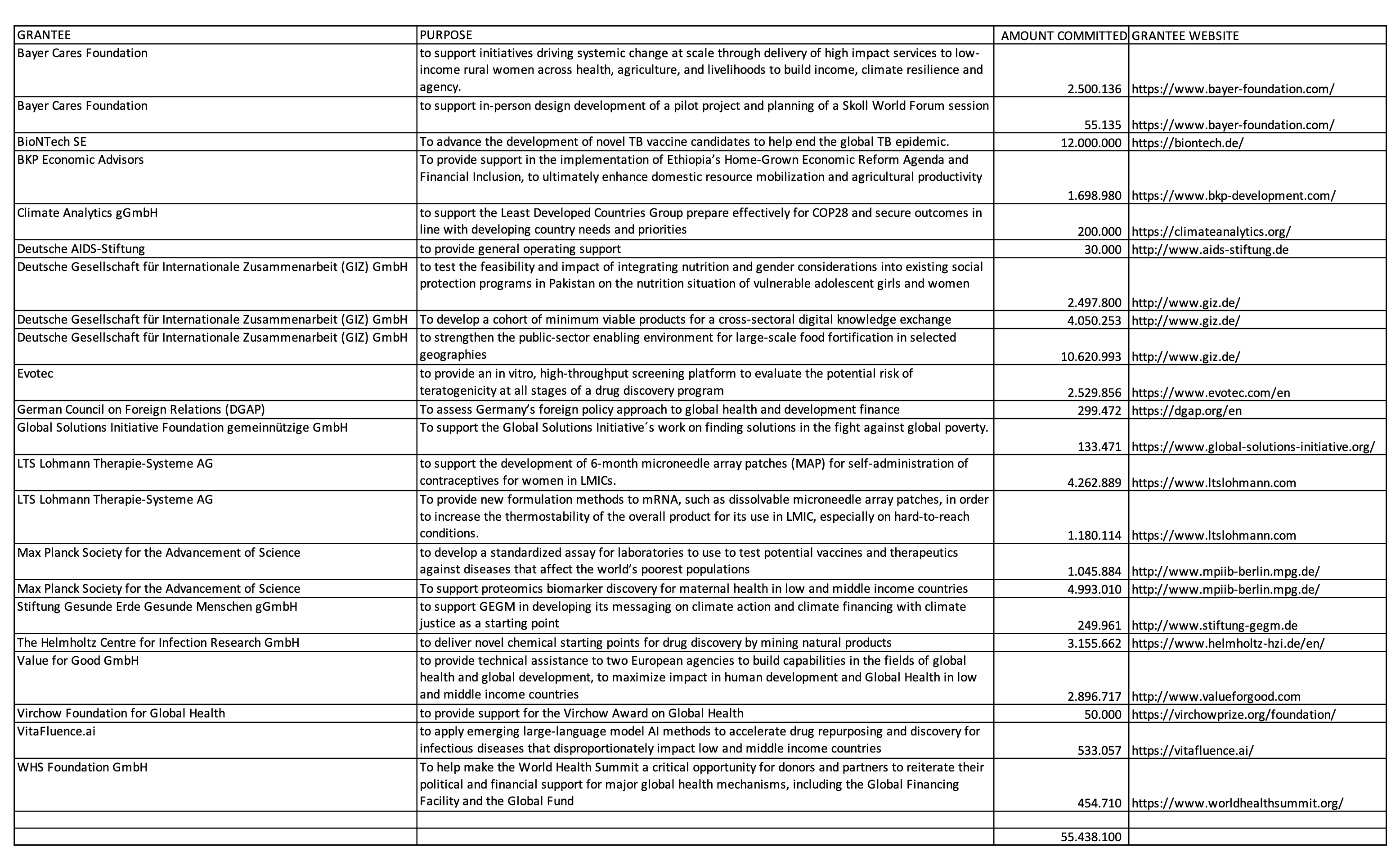
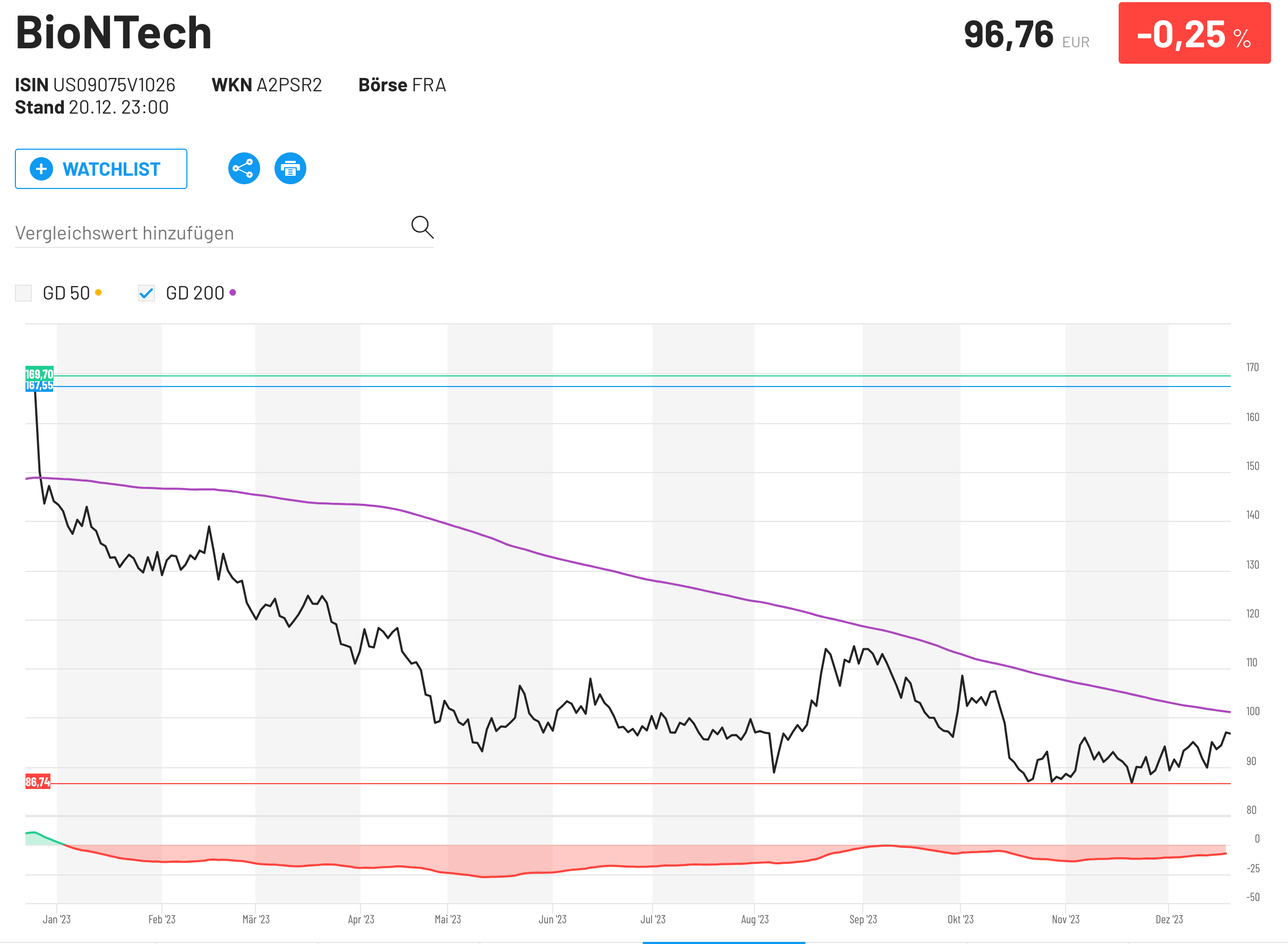
»… Für unbürokratische und leistungsorientierte Kooperationen zwischen allen Beteiligten plädierte auch der Medical Director von Biontech, Harald Gschaidmeier. Bei der Markteinführung der Impfstoffe habe Biontech mit sehr vielen lokalen Partnern wie etwa den Großhändlern, Apotheken und Hausärztinnen und Hausärzten zusammengearbeitet. Auch mit dem BMG war man im sehr intensiven Austausch. Dies habe gezeigt, was in Deutschland möglich ist, wenn viele Akteure unbürokratisch an einem Strang ziehen, so Gschaidmeier. „Bessere Pandemievorbereitung: Von COVID-19 lernen“ weiterlesen