Aus der Pressemitteilung auf investors.biontech.de vom 30.8.23
»Wichtige Sicherheitsinformationen
-
-
- Es wurden Fälle von Anaphylaxie berichtet. Für den Fall einer anaphylaktischen Reaktion nach der Verabreichung des Impfstoffs sollte immer eine angemessene medizinische Behandlung und Überwachung bereitstehen.
- Es besteht ein erhöhtes Risiko (<1/10.000 Fälle) einer Myokarditis (Entzündung des Herzmuskels) und Perikarditis (Entzündung des Herzbeutels) bei Personen, die COMIRNATY erhalten haben.
-
Diese Beschwerden können sich innerhalb weniger Tage nach der Impfung entwickeln und traten vornehmlich innerhalb von 14 Tagen nach der Impfung auf. Diese Beschwerden wurden häufiger nach Verabreichung der zweiten Impfdosis beobachtet sowie häufiger bei jüngeren Männern. Die verfügbaren Daten deuten darauf hin, dass sich der Verlauf der Myokarditis und Perikarditis nach der Impfung nicht von Myokarditis oder Perikarditis im Allgemeinen unterscheidet.
-
-
- Seltene Fälle von akuter peripherer Gesichtslähmung, seltenes Auftreten von Schlaflosigkeit, Hyperhidrose und nächtlichem Schwitzen; unbekanntes Auftreten von Parästhesie, Hypoästhesie, Erythema multiforme sowie starken Menstruationsblutungen und starken Schwellungen der Gliedmaßen und des Gesichtes wurden in der Praxis beobachtet.
- Im Zusammenhang mit der Impfung selbst können Angstreaktionen wie vasovagale Reaktionen (Synkopen), Hyperventilation oder Stressreaktionen (z. B. Schwindel, Herzklopfen, Anstieg der Herzfrequenz, Blutdruckveränderungen, Kribbeln und Schwitzen) auftreten. Stressbedingte Reaktionen sind vorübergehend und klingen von selbst wieder ab. Die Betroffenen sollten darauf hingewiesen werden, dass sie ihre Symptome dem Impfarzt melden sollten, damit dieser sie untersuchen kann. Es ist wichtig, dass Vorkehrungen getroffen werden, um Verletzungen durch Ohnmacht zu vermeiden.
- Die Impfung sollte verschoben werden, wenn Personen an einer akuten schweren fiebrigen Erkrankung oder einer akuten Infektion leiden. Eine leichte Infektion und/oder niedriges Fieber sollte die Impfung nicht verzögern.
- Wie bei anderen intramuskulären Injektionen sollte der Impfstoff bei Personen, die eine Therapie mit Antikoagulantien erhalten, oder bei Personen mit Thrombozytopenie oder einer Gerinnungsstörung (z. B. Hämophilie) mit Vorsicht verabreicht werden, da bei diesen Personen nach einer intramuskulären Verabreichung Blutungen oder Blutergüsse auftreten können.
- Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs wurden bei immungeschwächten Personen, einschließlich Personen, die eine immunsuppressive Therapie erhalten, nicht untersucht. Die Wirksamkeit von COMIRNATY, COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 kann bei immunsupprimierten Personen geringer sein.
- Wie bei jedem Impfstoff schützt die Impfung mit COMIRNATY, COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 möglicherweise nicht alle Empfänger des Impfstoffs. Personen sind möglicherweise erst 7 Tage nach ihrer zweiten Impfdosis vollständig geschützt.
- Nebenwirkungen, die während der klinischen Studien beobachtet wurden, sind nachfolgend hinsichtlich der Häufigkeit ihres Auftretens kategorisiert: sehr häufig (≥ 1/10), häufig (≥ 1/100 bis < 1/10), nicht häufig (≥ 1/1,000 bis < 1/100), selten (≥ 1/10,000 bis < 1/1,000), sehr selten (< 1/10,000).
- Sehr häufige Nebenwirkungen: Schmerzen und Schwellungen an der Injektionsstelle, Müdigkeit, Kopfschmerzen, Muskelschmerzen, Schüttelfrost, Gliederschmerzen, Durchfall, Fieber
- Häufige Nebenwirkungen: Rötungen an der Einstichstelle, Übelkeit, Übergeben
- Nicht häufige Nebenwirkungen: vergrößerte Lymphknoten (häufiger nach Auffrischungsimpfungen), Unwohlsein, Armschmerzen, Schlaflosigkeit, Juckreiz an der Injektionsstelle, allergische Reaktionen darunter Ausschläge oder Juckreiz, Schwächegefühl oder Energieverlust/Müdigkeit, verringerter Appetit, übermäßiges Schwitzen, Nachtschweiß
- Seltene Nebenwirkungen: vorübergehende halbseitige Gesichtslähmung, allergische Reaktionen wie Nesselsucht oder Schwellungen im Gesicht
- Sehr seltene auftretende Nebenwirkungen sind: Myokarditis (Entzündung des Herzmuskels) oder Perikarditis (Entzündung des Herzbeutels), die zu Atembeschwerden, Herzklopfen oder Brustschmerzen, Anaphylaxie, starke Schwellungen der geimpften Gliedmaßen führen kann; Schwellungen im Gesicht, Gefühl von Nadelstichen/Kribbeln, vermindertes Gefühlsempfinden oder Berührungsempfinden, Hautreaktion, die rote Punkte oder Flecken auf der Haut verursacht
- Eine große Anzahl von Beobachtungsdaten schwangerer Frauen, die im zweiten und dritten Trimester mit COMIRNATY geimpft wurden, haben keinen Anstieg nachteiliger Schwangerschaftsverläufe gezeigt. Zwar liegen derzeit nur wenige Daten zu den Schwangerschaftsergebnissen nach einer Impfung im ersten Trimester vor, doch wurde kein erhöhtes Risiko für eine Fehlgeburt festgestellt. COMIRNATY kann während der Schwangerschaft verabreicht werden. Es sind keine Auswirkungen auf das gestillte Neugeborene/Kleinkind zu erwarten, da die systemische Exposition der stillenden Frau gegenüber COMIRNATY vernachlässigbar ist. Beobachtungsdaten von Frauen, die nach der Impfung gestillt haben, zeigten keine erhöhten Nebenwirkungsrisiken für das gestillte Neugeborene/Kleinkind. COMIRNATY kann während der Stillzeit verabreicht werden.
- Bisher liegen keine Daten zur Verabreichung von COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 während der Schwangerschaft vor. Da die Unterschiede zwischen den Produkten auf die Spike-Protein-Sequenz begrenzt sind und es keine klinisch relevanten Unterschiede in der Reaktivität zwischen den variantenangepassten Versionen von COMIRNATY, die klinisch getestet wurden, gibt, kann COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 während der Schwangerschaft verwendet werden.
- Derzeit liegen keine Daten zur Verabreichung von COMIRNATY Original/ Omikron BA.1 oder COMIRNATY Original/ Omikron BA.4–5 während der Stillzeit vor. Beobachtungsdaten von Frauen, die nach der Impfung mit dem ursprünglich zugelassenen COMIRNATY-Impfstoff gestillt haben, zeigten keine erhöhten Nebenwirkungsrisiken für das gestillte Neugeborene/den Säugling. COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 kann während der Stillzeit verabreicht werden.
- Wechselwirkungen mit anderen Arzneimitteln oder die gleichzeitige Verabreichung von COMIRNATY oder COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 mit anderen Impfstoffen sind nicht untersucht worden.
- Tierversuche haben keinen Hinweis auf direkte oder indirekte schädliche Auswirkungen in Bezug auf Reproduktionstoxizität erbracht.
- Das Sicherheitsprofil einer Auffrischungsimpfung mit COMIRNATY Original/Omikron BA.1 bei Personen im Alter von 18 bis ≤ 55 Jahren wurde auf Basis einer Untergruppe von 315 Personen im Alter von 18 bis ≤ 55 Jahren extrapoliert, die nach drei COMIRNATY-Impfdosen eine vierte Auffrischungsimpfung mit 30-µg des Omikron BA.1 Impfstoffes erhalten haben. Die häufigsten Nebenwirkungen bei den Teilnehmerinnen und Teilnehmern im Alter von 18 bis ≤ 55 Jahren waren Schmerzen an der Injektionsstelle (> 70 %), Müdigkeit (> 60 %), Kopfschmerzen (> 40 %), Muskelschmerzen (> 30 %), Schüttelfrost (> 30 %) und Gelenkschmerzen (> 20 %).
- In einer Untergruppe der Phase-3-Studie erhielten 305 Erwachsene über 55 Jahren, die bereits drei Impfungen mit COMIRNATY erhalten hatten, 5 bis 12 Monate nach Erhalt der dritten Dosis eine Auffrischungsimpfung mit dem COMIRNATY Original/Omikron BA.1 Impfstoff. Teilnehmerinnen und Teilnehmer, die die Auffrischungsimpfung mit dem CORMINATY Original/Omikron BA.1 Impfstoff erhielten, wurden bis zum Datenstichtag am 16. Mai 2022 mindestens 1,7 Monate lang nachbeobachtet. Das Sicherheitsprofil der COMIRNATY/Omikron BA.1 Auffrischungsimpfung (vierte Impfdosis) war vergleichbar mit der dritten Auffrischungsimpfung von COMIRNATY (dritte Impfdosis). Die häufigsten Nebenwirkungen bei Teilnehmerinnen und Teilnehmern über 55 Jahren waren Schmerzen an der Injektionsstelle (> 60 %), Müdigkeit (> 40 %), Kopfschmerzen (> 20 %), Muskelschmerzen und Schüttelfrost (> 10 %).
- Das Sicherheitsprofil einer COMIRNATY Original/Omikron BA.4–5 Auffrischungsimpfung wurde aus den Sicherheitsdaten einer COMIRNATY Original/Omikron BA.1 Auffrischungsdosis, sowie den Daten der COMRINATY Original Auffrischungsimpfung abgeleitet.
- Die Dauer des Schutzes durch den Impfstoff ist derzeit noch unbekannt, da sie in den noch laufenden klinischen Studien ermittelt wird. Wie bei jedem Impfstoff schützt die Impfung mit COMIRNATY/Omikron BA.1 oder COMIRNATY/Omikron BA.4–5 möglicherweise nicht alle Empfänger des Impfstoffs.
- Die vollständigen Sicherheitsinformationen zu COMIRNATY, COMIRNATY Original/Omikron BA.1 und COMIRNATY Original/Omikron BA.4–5 sind in der zugelassenen Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage zu finden. Diese sind in allen Sprachen der Europäischen Union auf der Webseite der EMA zu finden…«
-
Auf der Biontech-Seite für Investoren gibt es auch die Rubrik "Finanzberichte".
Dort ist zu erfahren:
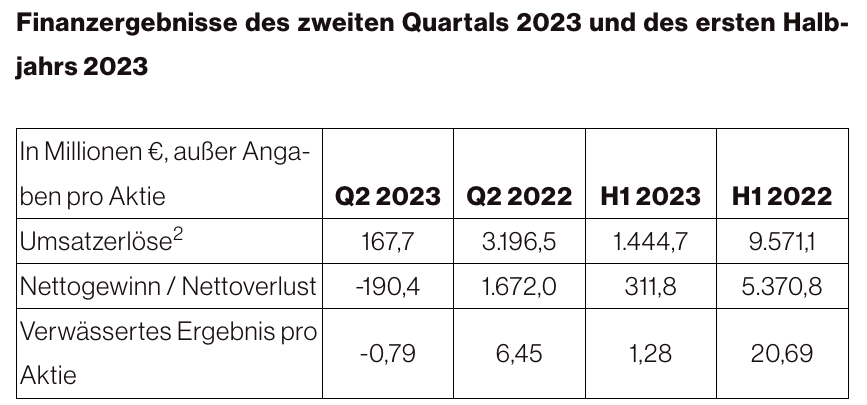
Zu diesen Milliardengewinnen trugen und tragen die Empfehlungen der Ständigen Impfkommission bei. Unter völliger Mißachtung der Herstellerangaben heißt es immer noch:
»Warum ist es weiterhin wichtig, sich entsprechend der STIKO-Empfehlung gegen COVID-19 impfen zu lassen?



Hier eine kurze Zusammenfassung bzgl. des Präparates gegen 20 Pneumococcen-Serotypen (PVC20 – als Präparate-Name Aprexxnar) aus der Seite http://www.impf-info.de des Kollegen Dr. Steffen Rabe (ehemaliger Vorsitzender von Ärzte für Individuelle Impfentscheidungen).
"Die randomisierten Zulassungsstudien beruhen ausschließlich auf serologischen Messungen von Antikörpern gegen die einzelnen Pneumokokken-Serotypen, nicht auf dem Verringern/Verhindern von durch Pneumokokken-Erkrankungen.
Verglichen mit PCV13 erreicht PCV20 bei den 13 gemeinsamen Serotypen nach der Definition der Studien "Nichtunterlegenheit", wobei die Titer bei 11 der 13 dennoch teilweise dennoch bis zu 30% unter denen nach PCV13 liegen (a‑t 2023). Letzteres betrifft auch den besonders problematischen Serotyp 3 (der häufig komplizierte Lungenentzündungen auslöst), die klinische Bedeutung dieser Unterschiede ist unklar.
Daten zur längerfristigen Immunogenität oder zu klinischen Wirksamkeit fehlen.
Für Pneumokokken-Impfstoffe ist nachgewiesen, dass die Gabe schmerzstillender/fiebersenkender Medikamente am Tag der Impfung die Immunantwort auf die Grundimmunisierung verringert."
Und bzgl. der Empfehlungen der STIKO, auf Krankenkasse.de veröffentlicht:
Wer glaubt diesen Handlanger denn überhaupt noch – hoffentlich nicht zu viele Menschen. Sie lügen wie gedruckt, denn diese Stoffe bieten weder einen Eigenschutz, noch einen Fremdschutz noch einen Schutz vor einem schweren Verlauf – dafür aber im Gegenzug viele, schwere und schwerste und tödliche Nebenwirkungen.
Na, das ist doch mal ein klasse Tausch: bringt nix gegen macht dich fertig.
Nach der STIKO gilt am besten für alle von Null bis Exitus: "Impfen Sie sich gegen alles, was der Arzt gerade im Kühlschrank hat" – und am besten mehrere Injektionen gleichzeitig, dann kann nachher auch keiner sagen / beweisen, was von welcher Suppe denn so an Nebenwirkungen kam.
Geschickt, so umgeht man ganz elegant evtl. Schadensansprüche.
Und natürlich kann man alles machen, was man will:
Sinnvolles, Unsinniges, Riskantes.
Nur sollte sich jeder immer bewusst sein und hinterfragen:
Wem hilft was bzw. wem nutzt was? Und in welcher Form (also Schutz oder nur Money)
Denn manche Dinge kann man auch nur einmal im Leben machen – für ein zweites Mal besteht dann keine Chance mehr (wie ja leider viel zu viele Menschen weltweit erleben mussten bzgl. der unsicheren, hochriskanten C.-Injektionen).
Allen noch einen schönen Sonntag
https://www.corodok.de/narziss-und-goldgrube/#comment-193312
Man oder frau muss nur die Pressemitteilung der "Impf"-Stoffhersteller ausdrucken und dann per Einschreiben oder per Email an die Stiko senden.
Vielleicht wissen die Stiko und RKI-Mitarbeiter gar nicht, was die Hersteller selbst zu ihren Produkten sagen.
Überraschung: Die Wirksamkeit von Impfstoffen hat die Produzenten noch nie interessiert! MFG
Naja, selbst ohne die bekannten Schummeleien (Teil-"Unblinding" von Studienteilnehmern): die Hersteller haben bei ihren "Zulassungsstudie" eben so gut wie alle "legalen" Möglichkeiten (z.T. sogar vorgegebene!) ausgereizt:
- Ausschluss von bestimmten Alters- und Risikogruppen
– Begrenzung der Anzahl der Versuchskaninchen (~20000)
– weitgehende Eliminierung der Kontrollgruppe nach x Monaten
– passgenaue Definitionen (z.B., dass man bis 14 Tage nach Zweitspritze noch als "ungeimpft" galt u.ä.)
Hinzu kam, für umme (steht das im geschwärzten Bereich der Verträge?):
– das Stakkato von Angstporno durch "passende" Presseberichte und Visualisierung einer angeblich fürchterlichen und brandneuen Gefahr mittels Maßnahmenterror ("Maskenpflicht")
– mediale "Impfwerbung"
– "Massenimpfungen" nach Quasi-Erpressung
– Verungl-"Impfung" von Kritikern und Skeptikern
– virtuelle Heiligsprechung der Hersteller
Pointe am Rande: "< 10000" sind also "sehr selten", macht in D bei ~60 Mio "vollständig Geimpften" also "< 6000"?
Für mitlesende Rechtgläubige: diesen Wert hat die "Anzahl gemeldeter intensivmedizinisch behandelter COVID-19-Fälle
Deutschland, Erwachsenen-Intensivstationen"
https://www.intensivregister.de/#/aktuelle-lage/zeitreihen
in 3 Jahren "Pandemie" nie erreicht, das dabei jeweils abzuziehende gute Drittel der "COVID-19-Intensivpatient*innen ohne Manifestation" nicht einmal berücksichtigt:
https://www.intensivregister.de/#/aktuelle-lage/manifestation
Blick zurück:
"Die schwedische Regierung hatte wie auch die deutsche Regierung Ende 2009 dazu aufgerufen, sich gegen die Schweinegrippe impfen zu lassen. In Schweden folgten 60 Prozent der Bevölkerung dem Rat"
https://www.spiegel.de/gesundheit/diagnose/schweinegrippe-impfung-schweden-entschaedigt-narkolepsie-patienten-a-1092175.html
demnach waren also 331 von ~6 Mio (entspricht ~ 0,55 von 10000) "sehr selten" (Untererfassungen nicht berücksichtigt).
Nicht auszudenken, was mit den o.e. "Werbemaßnahmen" dabei herausgekommen wäre.
Nachtrag aus
https://www.spiegel.de/gesundheit/diagnose/schweinegrippe-impfung-schweden-entschaedigt-narkolepsie-patienten-a-1092175.html
Wie dpa/SPIEGEL und PEI auch 2016 bereits "informierten":
"In Deutschland ließen sich nur rund acht Prozent der Bevölkerung impfen, auch die Zahl der möglichen Narkolepsie-Fälle liegt deutlich niedriger. Hierzulande wurden nach Angaben des Paul-Ehrlich-Instituts bis März 81 Betroffene registriert, bei denen es einen Zusammenhang mit der Impfung geben könnte".
Diese "nur rund acht Prozent" sind in absoluten Zahlen ~6,5 Mio (8% von damals ~82 Mio) etwas mehr als jene ~6 Mio (60 Prozent von damals ~10 Mio Einwohnern Schwedens).
Dass man in der BRD bis März 2016, also über 6 Jahre nach dem "kleinen Pieksen", nur "81 Betroffene registriert [hat], bei denen es einen Zusammenhang mit der Impfung geben könnte" muss nicht einmal eine besondere Untererfassung (gegenüber den viermal so hohen schwedischen Zahlen) bedeuten, da man davon ausgehen kann, dass die "rund acht Prozent" deutschen "Impflinge" im Gegensatz zu Schweden eher nicht repräsentativ gewesen sein dürften, und sich wohl überwiegend auf die impffreundlichen Ü‑70er beschränkte.
Und, abgesehen von den altersgemäß häufiger auftretenden (manchmal auch plötzlichen und unerwarteten) Todesfällen in dieser Generation: wer würde (ohne alltägliche mediale Unterstützung) schon den Verdacht hegen, dass bleierne Müdigkeit Symptom einer "sehr seltenen" Krankheit sein könnte?
@Kassandro: Etliche Beiträge zur Schweingrippe und der Rolle Drostens dabei gibt es auch hier: https://www.corodok.de/?s=schweinegrippe
Die Berufslügner der Tagesschau "berichten":
https://www.tagesschau.de/wissen/gesundheit/corona-impfung-177.html
Dazu passt: "Listerien: Rückrufaktion für Käse aus dem Thurgau"
https://www.swr.de/swraktuell/baden-wuerttemberg/friedrichshafen/rueckruf-von-kaese-aus-dem-thurgau-wegen-listerien-100.html
hier fehlt eine blaue hervorhebung:
"Personen sind möglicherweise erst 7 Tage nach ihrer zweiten Impfdosis vollständig geschützt."
vor was ist man nach 7 tagen nach der zweiten impfung möglicherweise vollständig geschützt?
was für ein krimineller Blödsinn Biontech von sich gibt. die haben gar Nichts untersucht
Ob mit oder ohne Untersuchung und Studie von unterschiedlichen Bevölkerungsgruppen, die Gentherapeutika sind hochtoxisch. Zum einen als Gentherapeutika aufgrund der (notwendigen) toxischen Inhaltsstoffe, was seit Jahrzehnten und vollkommen bekannt ist. Zum anderen aufgrund des Spike-Proteiens.
Wer die "Impfung" als Schutz ansieht und den Schuss noch nicht gehört hat, der wird munter weiter seinen Körper mit toxischen Gentherapeutika vollpumpen lassen. Zur Freude der Pharmaindustrie, die auch an den "impf"bedingten ursächlichen Erkrankungen (Krebs, Autoimmunerkrankungen etc.) gigantisch verdient. (Wo bleiben eigentlich die erfolgreichen gentherapiebasierten Krebstherapien?)
Mit Logik kommt man bei einer auf Propaganda trainierten Bevölkerung leider nur begrenzt weiter. "Der Staat" meint es ja nur gut mit uns.
UKHSA · UK Health Security Agency. GOV.UK · UK Government information.
22.09.2023 (Last updated).
·
COVID-19 variants identified in the UK—Latest updates on SARS-CoV‑2 variants detected in the UK.
UKHSA releases latest data on variant BA.2.86 [ Pirola ]
The UK Health Security Agency (UKHSA) has published its latest variant technical briefing containing updated analysis of the emergent variant BA.2.86. BA.2.86 continues to transmit within the UK, with sporadic cases identified in most regions.
The briefing contains early laboratory data from a number of scientific organisations around the UK, including UKHSA’s own Vaccine Development and Evaluation Centre (VDEC), the University of Oxford, the Glasgow Centre of Virus Research and the Pirbright Institute. This early data indicates that BA.2.86 is no more likely to evade existing antibodies than XBB.1.5, another variant that has been circulating widely in the UK.
While the available data remains limited, there is currently no evidence to suggest that BA.2.86 infection is more likely to make people seriously ill than currently-circulating variants, while vaccination is likely to provide continued protection.
UKHSA will continue to monitor vaccine effectiveness in the population throughout the winter and will publish updated analysis in due course.
Professor Susan Hopkins, Chief Medical Advisor, UKHSA said:
"While this is still very early data and more research is needed before we can be certain, it is encouraging to see an initial indication that BA.2.86 demonstrates similar levels of antibody escape compared to other variants circulating in the UK. The available data is too limited to draw conclusions about the severity of the illness it causes, but there is so far no evidence to suggest that it is more likely to make people seriously ill than other Omicron variants in circulation."
"The autumn vaccination programme started this month, and this new data shows once again how important it is that the most vulnerable among us are fully vaccinated in order to receive the greatest possible protection. I urge everyone eligible to come forward for their next dose as soon as they are called."
(…)
BA.2.86 was first identified in August and, as of 18 September, 137 cases have been sequenced in 15 countries: Australia, Canada, Denmark, France, Germany, Israel, Japan, Portugal, South Africa, South Korea, Spain, Sweden, Switzerland, the UK, and the US. As of 18 September, there were 54 confirmed cases in the UK, 48 in England and 6 in Scotland. No cases have been identified in Wales or Northern Ireland. Of the 48 cases in England, 30 were identified as part of a care home outbreak investigation in the East of England, while the other 18 were identified through routine genomic surveillance.
Of the 48 cases, 10 cases were hospitalised, 2 were tested in an emergency department, and 6 cases have unknown hospitalisation status. (…)
The advice remains unchanged; if you have any symptoms of respiratory infection, you should limit your contact with other people as much as possible, especially the elderly and those with existing medical conditions.
The autumn vaccination campaign for COVID-19 and flu is under way for those people at higher risk.
UKHSA is urging everyone who is offered a vaccination to come forward and take it up as soon as possible.
gov.uk/government/news/covid-19-variants-identified-in-the-uk-latest-update
·
Professor Susan Hopkins is the Chief Medical Advisor at the UK Health Security Agency (UKHSA). In this capacity she leads the Clinical and Public Health Group whose objective is to provide professional health security, clinical and public health leadership.
Susan is also a Professor of Infectious Diseases and Health Security at University College London and continues to work clinically as a consultant in Infectious Diseases and Microbiology at the Royal Free London NHS Foundation Trust.
gov.uk/government/people/susan-hopkins
·
“STOP COVAX.”
„Was passiert, wenn die DNA in den Zellkern eindringt?“
INTERVIEW MIT BRIGITTE KÖNIG am 28. September 2023
"In Chargen des Impfstoffs Comirnaty wurde wiederholt Fremd-DNA entdeckt. Wissenschaftler machen sich Sorgen. Doch das Bundesgesundheitsministerium wiegelt ab. „Cicero“ sprach mit der Mikrobiologin und Immunologin Brigitte König, die den Impfstoff untersucht hat. .."
https://www.cicero.de/kultur/corona-impfstoff-verunreinigungen-dna-comirnaty ( Bezahlschranke)
Klassischer Fall von „Stille Post“:
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs wurden bei immungeschwächten Personen… nicht untersucht.«
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs wurden bei immungeschwächten Personen durch Studien bislang nicht ausgeschlossen.«
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs liegt bei immungeschwächten Personen nach aktueller Studienlage im Bereich des Möglichen.«
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs ist bei immungeschwächten Personen nach aktueller Studienlage anzunehmen.«
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs ist bei immungeschwächten Personen durch die aktuelle Studienlage gedeckt.«
»Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs ist bei immungeschwächten Personen durch die aktuelle Studienlage sichergestellt.«
Daher: Impfpflicht für das unsolidarische Verweigererpack!
"wirksame und gut verträgliche Impfstoffe in ausreichender Menge"
02.10.2023, 13:33 Uhr – Senatsverwaltung für Wissenschaft, Gesundheit und Pflege
Start der Grippesaison – Mit Impfung geschützt durch Herbst und Winter
Mit dem Beginn der kalten und wechselhaften Jahreszeit muss wieder mit verstärktem Auftreten akuter Atemwegserkrankungen gerechnet werden. Dazu zählen nicht nur die „gewöhnliche“ Erkältung und fieberhafte „grippale“ Infekte, sondern auch Fälle echter Virusgrippe (Influenza) und COVID-19-Erkrankungen. Gerade Influenza und COVID-19 verursachen eine erhebliche Krankheitslast in der Bevölkerung, vor allem bei Älteren und Menschen mit bestimmten Vorerkrankungen (z.B. Atemwegs‑, Herz-Kreislauferkrankungen, geschwächtes Immunsystem). Für den Schutz dieser besonders vulnerablen Personen stehen wirksame und gut verträgliche Impfstoffe in ausreichender Menge zur Verfügung.
Dr. Ina Czyborra, Senatorin für Wissenschaft, Gesundheit und Pflege: „Eine Impfung schützt Sie und Ihre Angehörigen vor schweren Krankheitsverläufen. Sie können damit auch eine Überlastung des Gesundheitswesens verhindern. Nutzen Sie außerdem die Gelegenheit, Ihren Impfschutz auf Aktualität und Vollständigkeit überprüfen zu lassen. “
Die Ständige Impfkommission (STIKO) beim Robert Koch-Institut (RKI) empfiehlt die jährliche Influenzaimpfung aktuell für:
• Personen ab einem Alter von 60 Jahren
• Personen mit erhöhter gesundheitlicher Gefährdung infolge eines Grundleidens
• Schwangere ab dem 2. Schwangerschaftsdrittel, bei erhöhter gesundheitlicher Gefährdung schon im ersten Drittel
• Bewohner von Alten- oder Pflegeheimen
• Personen, die als mögliche Infektionsquelle im selben Haushalt Lebende oder von ihnen betreute Risikopersonen gefährden könnten
• Personen mit erhöhtem berufsbedingten Infektionsrisiko (z.B. medizinisches Personal, Personen in Einrichtungen mit umfangreichem Publikumsverkehr)
• Weitere Informationen: RKI – Influenza – Antworten auf häufig gestellte Fragen zur Schutzimpfung gegen Influenza
Eine Auffrischimpfung zum Schutz vor COVID-19 empfiehlt die STIKO aktuell für:
• Personen ab einem Alter von 60 Jahren
• Kinder ab einem Alter von 6 Monaten mit Grunderkrankungen, die mit einem erhöhten Risiko für einen schweren COVID-19-Verlauf einhergehen können
• Personen mit einem erhöhten arbeitsbedingten Infektionsrisiko im medizinischen oder pflegerischen Bereich mit direktem Patientenkontakt
• enge Kontaktpersonen von Personen, bei denen durch die COVID-19-Impfung vermutlich keine schützende Immunantwort erzielt werden kann
Für Personen mit STIKO-Empfehlung sind diese Impfungen Pflichtleistungen der gesetzlichen Krankenversicherung und damit für Versicherte kostenlos. Die Influenza-Impfung kann gleichzeitig mit einer COVID-(Auffrisch-)Impfung verabreicht werden. Die Impfungen werden von vielen Hausärztinnen und –ärzten, aber auch von Ärztinnen und Ärzten anderer Fachgruppen angeboten. Darüber hinaus bieten auch Apotheken in ganz Berlin diese Impfungen an.
Weitere Informationen:
RKI – Impfen – COVID-19 und Impfen: Antworten auf häufig gestellte Fragen
Pressekontakt: Sarah Oswald
Als eines der weltweit führenden innovativen biopharmazeutischen Unternehmen sehen wir es als unsere Verantwortung, mit Gesundheitsversorgern, Regierungen und lokalen Gemeinschaften zusammenzuarbeiten, um den Zugang zur Gesundheitsversorgung auf der ganzen Welt zu unterstützen.
=====
Zitat, Pressemitteilung des Herstellers.
Übersetzt:
Wir manipulieren, beeinflussen, versehen mit Sponsorengeldern alle Gesundheitsminister, ‑ministerinnen, Regierungen und örtlichen Kommunen, um unsere Produkte (für unsere Firmen gewinnbringend) weiter an Millionen Versuchspersonen zu testen. Bei denen erheben wir anschließend "Beobachtungsdaten". Die Beobachtungsdaten der "Geimpften" liefern uns wichtige neue Erkenntnisse.
Vielen Dank an alle bereits mit unseren Produkten behandelten Personen, die sich kostenlos weltweit unseren Beobachtungsreihen in den letzten drei Jahren zur Verfügung gestellt haben, eventuell auch ein Eis am Stiel oder eine Bratwurst als Honorar genießen durften.
Sollten Sie eine tödliche oder krank machende Charge verabreicht bekommen haben, tut uns das Leid, doch trösten Sie sich: Ihre Beobachtungsdaten sind sehr wertvoll, denn damit können wir Ihr Leid, Ihr langsames oder schnelles Sterben je nach Charge beobachten, messen, auswerten. Wir können das Wissen um die schweren Stufen Ihrer Impfschäden in unsere neu zu entwickelnden MOD-RNA-Präparate integrieren. Andere, die sich behandeln lassen nach Ihnen, profitieren davon, darauf können Sie sich verlassen.
Also sorgen Sie sich nicht, denn Sie haben etwas wirklich sehr Wertvolles für die Gemeinschaft und für Ihr soziales Umfeld getan. Sie haben sich als Versuchskaninchen gratis zur Verfügung gestellt. Auch haben Sie indirekt einen wertvollen Beitrag zur Initiative "Keine Labor-Tests an Tieren" geleistet und viele Labor-Hamster, Mäuse, Ratten, Katzen oder Laborhunde vor dem Tod und schwersten Schäden bewahrt.
Respekt und nochmals vielen Dank dafür: Ihre "Impf"-Stoff-Hersteller
https://tierversuchsfrei.peta-approved.de/
Das ist gut. Tierversuchsfrei. Prima. Geben Sie den Pharma- und/oder "Impf"-Stoffhersteller Ihrer Wahl ein. Und überzeugen Sie sich von seiner Tierfreundlichkeit. Ähm, nein, da geht es nur um Kosmetik. Also, nur um äußerliche Anwendungen, nicht um innere mögliche Zerstörungen im Gewebe von Menschen.
«Staatsfeinde», «Schweinehunde», «Bekloppte» – vor zwei Jahren überboten sich Qualitätsmedien mit Tiraden gegen Massnahmenkritiker und Impfskeptiker (02.10.2023)
https://www.nzz.ch/feuilleton/corona-medien-staatsfeinde-ungeimpfte-lauterbach-ld.1757085
02.10.2023.
The Nobel Assembly at Karolinska Institutet has today decided to award the 2023 Nobel Prize in Physiology or Medicine jointly to Katalin Karikó and Drew Weissman for their discoveries concerning nucleoside base modifications that enabled the development of effective mRNA vaccines against COVID-19
The discoveries by the two Nobel Laureates were critical for developing effective mRNA vaccines against COVID-19 during the pandemic that began in early 2020. Through their groundbreaking findings, which have fundamentally changed our understanding of how mRNA interacts with our immune system, the laureates contributed to the unprecedented rate of vaccine development during one of the greatest threats to human health in modern times (…)
https://www.nobelprize.org/prizes/medicine/2023/press-release/
The Nobel Prize in Physiology or Medicine 2023 was awarded jointly to Katalin Karikó and Drew Weissman "for their discoveries concerning nucleoside base modifications that enabled the development of effective mRNA vaccines against COVID-19"
https://www.nobelprize.org/prizes/medicine/2023/summary/
·
All nomination records for a prize are sealed for 50 years from the awarding of the prize.
https://en.wikipedia.org/wiki/Nobel_Prize
Geheimhaltungspflicht für 50 Jahre
https://de.wikipedia.org/wiki/Nobelpreis
The names of the nominees and other information about the nominations and selection process cannot be revealed until 50 years later.
https://www.nobelprize.org/nomination/medicine/
·
mRNA medicines we are currently developing · Moderna
modernatx.com/en-US/research/product-pipeline
·
“mοdRNA harms or kills.”
nucleoside-modified mRNA ( mοdRNA )
https://en.wikipedia.org/wiki/Nucleoside-modified_messenger_RNA
“mοdRNA schädigt oder tötet.”
Nukleosid-modifizierte mRNA ( mοdRNA )
https://de.wikipedia.org/wiki/Nukleosid-modifizierte_mRNA
Empfehlungen und Vorschläge des Amerikanischen Kollegium der Geburtshelfer und Gynäkologen (ACOG) zum Überreden von Schwangeren zur Spritze mit den experimentellen gentechnischen C19 Substanzen:
COVID-19 Impfstoffe und Schwangerschaft: Gesprächsleitfaden
Wichtige Empfehlungen und Botschaften für Kliniker
https://www.acog.org/covid-19/covid-19-vaccines-and-pregnancy-conversation-guide-for-clinicians
Key Recommendations
The American College of Obstetricians and Gynecologists (ACOG) strongly recommends that pregnant individuals be vaccinated against COVID-19.
Vaccination may occur in any trimester, and emphasis should be on vaccine receipt as soon as possible to maximize maternal and fetal health.
For patients who do not receive any COVID-19 vaccine, the discussion should be documented in the patient’s medical record. During subsequent office visits, obstetrician–gynecologists should address ongoing questions and concerns and offer vaccination again.
COVID-19 vaccines may be administered simultaneously with other vaccines, including within 14 days of receipt of another vaccine. This includes vaccines routinely administered during pregnancy, such as the influenza and Tdap vaccines.
Wichtige Empfehlungen
Das American College of Obstetricians and Gynecologists (ACOG) empfiehlt nachdrücklich, dass sich Schwangere gegen COVID-19 impfen lassen.
Die Impfung kann in jedem Trimester erfolgen, wobei der Schwerpunkt darauf liegen sollte, dass der Impfstoff so bald wie möglich verabreicht wird, um die Gesundheit von Mutter und Kind zu maximieren.
Bei Patientinnen, die nicht gegen COVID-19 geimpft werden, sollte das Gespräch in der Krankenakte der Patientin dokumentiert werden. Bei den folgenden Arztbesuchen sollten die Gynäkologen und Geburtshelfer auf bestehende Fragen und Bedenken eingehen und die Impfung erneut anbieten.
COVID-19-Impfstoffe können gleichzeitig mit anderen Impfstoffen verabreicht werden, auch innerhalb von 14 Tagen nach Erhalt eines anderen Impfstoffs. Dies gilt auch für Impfstoffe, die während der Schwangerschaft routinemäßig verabreicht werden, wie z. B. Grippe- und Tdap-Impfstoffe.
So weit, so schlimm. Es geht dann munter weiter, auch in den weiterführenden Links auf dieser Webseite.
Das ist ein echt schlimmer Vakzinisten-Alptraum.
Selbst wenn das hier niemand mehr liest und es irgendwann im weltweiten Datenmüllberg wieder verschwindet, ist es mir doch ein Anliegen, dieses aus blanken Entsetzen wenigstens hier zu dokumentieren.
Danke! Das ist sehr bedrückend.
Das ist Psy_Op = Psychological Operation. Im Grunde ist der komplette Blog seit 2020 ein Blick in die Abgründe der menschlichen, bösen Seelen. Manchmal aufgelockert durch schwarzen, bissigen Humor, doch das, was man / frau hier an Aufzeichnungen, Abschriften, Zitaten solcher Vakzinisten und ihrer Helfer in den kritischen Artikeln und ebenso kritischen Kommentaren findet, braucht oft sehr starke Nerven beim Lesen.
Geschäft.
Dr. Mattias Desmet · EU Parliament.
13.09.2023.
Prof. Mattias Desmet, Belgian Psychologist, testified at the hearing in the European Parliament in Strasbourg concerning the World Health Organization.
https://odysee.com/@DenG:7/Mattias-Desmet-EU-Parliament:c
·
September 13, 2023 European Parliament Session
“Health and Democracy under WHO’s new proposed rules, benefits and risks for the civil society”
— Peter McCullough MD MPH (/məˈkʌlə/, Peter Andrew McCullough, Peter A. McCullough.)
petermcculloughmd.substack.com/p/one-bio-pharmaceutical-complex-two
·
Expert Hearing in the EU Parliament · 13.09.2023, room de Madriaga s7 (SdM = Le bâtiment Salvador de Madariaga).
Hosting MEPs:
MEP Christine Anderson (Germany)
MEP Mislav Kolakušić (Croatia)
MEP Ivan Sinčić (Croatia) (Ivan Vilibor Sinčić)
MEP Cristian Terheş (Romania) (Cristian-Vasile Terheş)
MEP Virginie Joron (France)
christineanderson.eu/en/expert-hearing-in-the-eu-parliament-13–09-2023–1430-1630-cet/
·
Cristian Terheş
(Zu Terheş s. u.: Pfizer, blanked out pages … Over 100 blacked out pages.)
(Parlement européen, Strasbourg.)
europarl.europa.eu/meps/de/197655/CRISTIAN_TERHES/home
europarl.europa.eu/meps/de/197655/CRISTIAN_TERHES/main-activities/plenary-speeches
·
13. September 2023 (Kettner).
(…) Heute findet im EU-Parlament eine Expertenanhörung statt, die sich mit den neuen, von der WHO vorgeschlagenen Regeln befasst.
Expertenanhörung im EU-Parlament
Die Expertenanhörung wird von zahlreichen Experten aus dem Bereich der Medizin und des Rechts besucht, darunter:
• Philipp Kruse, Rechtsanwalt (Schweiz)
• Dr. Renate Holzeisen, Rechtsanwältin (Italien)
• Prof. Dr. Michael Geistlinger, a.o. Universitätsprofessor i. R. für Völkerrecht, Europarecht (Österreich)
• Dr. Beate Sibylle Pfeil, Rechtswissenschaftlerin, Expertin für Völker- und Minderheitenrecht (Deutschland)
• Dr. Maria Hubmer-Mogg, Medizinerin (Österreich)
• Univ. Prof. Dr. Andreas Sönnichsen, Mediziner (Österreich)
• Dr. Peter Mc Cullough, Mediziner (USA)
• Prof. Dr. Mattias Desmet, Professor für Klinische Psychologie (Belgien)
• Dr. David Martin, CEO M‑CAM (USA)
kettner-edelmetalle.de/news/wachsender-widerstand-gegen-who-pandemievertrag-expertenanhorung-im-eu-parlament-13–09-2023
·
Das Europäische Parlament (inoffiziell auch Europaparlament oder EU-Parlament; kurz EP; lateinisch Parlamentum Europaeum) mit offiziellem Sitz in Straßburg ist das Parlament der Europäischen Union (Art. 14 EU-Vertrag).
de.wikipedia.org/wiki/Europäisches_Parlament
The European Parliament (EP) is one of the legislative bodies of the European Union and one of its seven institutions. Together with the Council of the European Union (known as the Council and informally as the Council of Ministers), it adopts European legislation, following a proposal by the European Commission. The Parliament is composed of 705 members (MEPs). It represents the second-largest democratic electorate in the world (after the Parliament of India), with an electorate of 375 million eligible voters in 2009.
en.wikipedia.org/wiki/European_Parliament
·
Pfizer, blanked out pages
21.10.2022, Dr. John Campbell.
Pfizer / European commission vaccine contracts, over 100 blanked out pages. This is how they were disclosed to us (MEP Cristian Terheş). Over 100 blacked out pages.
https://www.youtube.com/watch?v=HnSnQor8zDY
@Edward von Roy: Auch wenn gerne der Anschein erweckt wird – diese Veranstaltung war keine des EU-Parlaments, sondern von 5 Abgeordneten.
@aa: Richtig, das ist so.
Möglicherweise sind bereits, oder werden noch, alle einzelnen Vorträge vom 13.09.2023 („HEALTH & DEMOCRACY under WHO’s new proposed rules—Benefits and Risks for the Civil Society“ ) an einem Ort dokumentiert. Hier jedenfalls findet sich ein weiterer Redebeitrag.
Dr. David E. Martin – 13. September 2023, Strasbourg
https://t.me/s/MAHUMO21?before=4830
https://vimeo.com/865636929/0f11bf7e47?share=copy
https://www.bitchute.com/video/aTC9si4KOD83/
"Schützt eure Säuglinge und Kinder vor der Covid-19-Spritze!"
Emotionaler Appell von Dr. Gunter Frank:
https://www.alexander-wallasch.de/gesellschaft/emotionaler-appell-von-dr-gunter-frank-schuetzt-eure-saeuglinge-und-kinder-vor-der-covid-19-spritze
Was sie uns nicht sagten: mRNA-Nobelpreisträger warnt vor Blutgerinnsel und anderen Impf-Nebenwirkungen:
https://uncutnews.ch/was-sie-uns-nicht-sagten-nobelpreistraeger-warnt-vor-mrna-impfstoff-nebenwirkungen/
@Esgehtwiederlos: Die zentrale Aussage dazu in der Arbeit von Weissman et al:
»Während präklinische Studien zu großem Optimismus hinsichtlich der Aussichten und Vorteile von mRNA-basierten Impfstoffen geführt haben, haben zwei neuere klinische Berichte zu gedämpfteren Erwartungen geführt. In beiden Studien war die Immunogenität beim Menschen bescheidener als aufgrund von Tiermodellen erwartet, ein Phänomen, das auch bei DNA-basierten Impfstoffen beobachtet wurde, und die Nebenwirkungen waren nicht unbedeutend. Wir weisen darauf hin, dass diese Studien nur zwei Varianten von mRNA-Impfstoffplattformen darstellen und dass es erhebliche Unterschiede geben kann, wenn die Expressions- und Immunstimulationsprofile des Impfstoffs verändert werden. Weitere Forschungsarbeiten sind erforderlich, um festzustellen, wie verschiedene Tierarten auf mRNA-Impfstoffkomponenten und Entzündungssignale reagieren und welche Wege der Immunsignalisierung beim Menschen am wirksamsten sind...
Umfangreiche Grundlagenforschung im Bereich der RNA-, Lipid- und Polymerbiochemie hat die Umsetzung von mRNA-Impfstoffen in klinische Studien ermöglicht und zu einem erstaunlichen Investitionsvolumen in mRNA-Impfstoffunternehmen geführt. Das 2010 gegründete Unternehmen Moderna Therapeutics hat fast 2 Milliarden US-Dollar an Kapital aufgebracht und plant die Vermarktung von mRNA-basierten Impfstoffen und Therapien. Die US-amerikanische Biomedical Advanced Research and Development Authority (BARDA) hat Moderna Unterstützung für die klinische Bewertung eines vielversprechenden nukleosidmodifizierten mRNA-Impfstoffs gegen das Zika-Virus zugesagt (NCT03014089). In Deutschland verfügt die CureVac AG über ein wachsendes Portfolio an therapeutischen Zielmolekülen, das sowohl Krebs als auch Infektionskrankheiten umfasst, und BioNTech entwickelt einen innovativen Ansatz für eine personalisierte Krebsmedizin mit mRNA-Impfstoffen. Die Umsetzung von Grundlagenforschung in klinische Tests wird auch durch die Kommerzialisierung von maßgeschneiderten GMP-Produkten durch Unternehmen wie New England Biolabs und Aldevron beschleunigt. Schließlich stimmt die kürzlich erfolgte Gründung der Coalition for Epidemic Preparedness Innovations (CEPI) sehr optimistisch für künftige Reaktionen auf neu auftretende Virusepidemien. Diese multinationale öffentliche und private Partnerschaft will 1 Milliarde Dollar aufbringen, um plattformbasierte Impfstoffe, z. B. mRNA, zu entwickeln, mit denen aufkommende Epidemien schnell eingedämmt werden können...«
Übersetzt aus dem Englischen, ohne Fußnoten und Links. (https://www.nature.com/articles/nrd.2017.243.pdf)
aus o.g.
https://investors.biontech.de/de/news-releases/news-release-details/pfizer-und-biontech-erhalten-positive-chmp-empfehlung-fuer‑4
Offenlegungshinweis von Pfizer
Die in dieser Pressemitteilung enthaltenen Informationen entsprechen dem
Stand vom 30. August 2023.
Pfizer übernimmt keine Verpflichtung,
die in dieser Mitteilung enthaltenen zukunftsgerichteten Aussagen
aufgrund neuer Informationen oder zukünftiger Ereignisse oder Entwicklungen
zu aktualisieren.
Auszug
Ist die neue Arzneimittelwerbung von BioNTech staatlich genehmigt?
Die neue Impfkampagne richtet sich an Menschen im Alter Ü‑60. 32 Millionen Menschen soll dies laut einer neuen Plakatkampagne betreffen.
Aber natürlich nicht ausschließlich, dazu gesellen sich für eine jährliche Spritze noch Bewohner in einer Senioreneinrichtung, „Personen ab 6 Monaten mit bestimmten Grunderkrankungen“ und natürlich darf auch das medizinische Personal nicht fehlen.
Die einzelnen Grunderkrankungen werden dann gerne auf der dazugehörigen Website detailliert erläutert. Bis auf das massive Übergewicht könnten alle auch eine Impfnebenwirkungen von vergangenen Impfkampagnen sein.
Nun stellt sich Rechtsanwältin Röhrig die Frage, ob sich BioNTech mit dieser Plakatwerbung über das grundsätzliche Verbot des Heilmittelerwerbsgesetzes hinwegsetzt. Ist die Arzneimittelwerbung von BioNTech also erlaubt?
Beitragsdatum 29. September 2023
https://corona-blog.net/2023/09/29/ist-die-neue-arzneimittelwerbung-von-biontech-staatlich-genehmigt/
@ob sich BioNTech…: Danke, aufgegriffen in https://www.corodok.de/nun-werbekampagne-biontech/.
https://www.corodok.de/o‑ton-biontech/#comment-193502
Zumindest ist das aber durchschaubar. Unter dem Plakat / unter dem Film steht gut lesbar: eine Initiative von BionTech. Das ist eindeutig Werbung. (Ob juristisch möglich, ist eine andere Frage.)
Aber ich als dummes blindes Huhn oder Versuchskaninchen, das damit in die nächsten pharmazeutischen Versuchsreihen eingebaut werden soll, kann das als solche erkennen. Und würde einfach mal sagen: soll doch jeder werben, wofür er oder sie will. Selbst wenn sie das stündlich in den Radionachrichten, jeden Abend kurz vor der ARD-Tagesschau bringen – ich sehe, das ist Werbung und kann einfach das Radio oder den Fernseher ausschalten. Diese "Impf"-Stoffhersteller können das auch an Plakaten an Bushaltestellen und in U‑Bahnhöfen aufhängen, an Litfass-Säulen, mir egal. Es ist nur Werbung. Ich sehe dann woanders hin, es interessiert mich nicht.
Ich will nur nicht, dass subtile Werbung getarnt als "Empfehlung der Stiko, des Gesundheitsministeriums" mich und andere verunsichert. "Hausärzte rufen zur Coronaschutzimpfung auf." Interessiert mich auch nicht. Solange ich den Durchblick habe, worum es geht, nämlich um Werbung für irgendwelche pharmazeutischen Produkte. Wer jetzt immer noch drauf reinfällt und hinterher mit Nebenwirkungen kämpf, tut mir leid, aber ist mir absolut egal.
Zigarettenwerbung hat mich auch nie interessiert, ich WILL einfach nicht Qualm einatmen, Werbung für Whiskey oder Vodka interessiert mich auch nicht, wenn ich lieber KEINEN hochprozentigen Alkohol kaufe, sondern nur mal Weißwein oder ein 6er Pack Mai-Ur-Bock. Und wenn ich nur Bananensaft kaufe, ignoriere ich die Whiskey-Werbung sowieso.
Wechselwirkungen mit anderen Arzneimitteln oder die gleichzeitige Verabreichung von COMIRNATY oder COMIRNATY Original/Omikron BA.1 oder COMIRNATY Original/Omikron BA.4–5 mit anderen Impfstoffen sind nicht untersucht worden.
*****************************************
Noch einmal das Originalzitat eines Covid-Impfstoff-Herstellers.
https://www.krankenkassen.de/dpa/444274.html
Diese Meldung stammt vom Sonntag, 19. November 2023. Ist das jetzt Werbung oder Irreführung oder was für ein "Aufruf" soll das sein?
Zitat:
Die Impfungen könnten auch kombiniert werden: «Linker Arm Grippe, rechter Arm Corona», sagte Gassen den Zeitungen.
Zitat Ende.
Der "Aufrufende" Gassen sagt nicht: Die "Impfungen" müssen kombiniert werden, sondern wählt den vorsichtigen Konjunktiv "könnten". Dennoch: ist es fahrlässig, so was zu fordern oder auch nur ansatzweise vorzuschlagen? Oder ist es schon Absicht, die Ahnungslosen zu schädigen, wenn doch der Hersteller überhaupt noch nicht untersucht hat, wie eben genau diese Wechselwirkungen unterschiedlicher Produkte sind?
COMIRNATY, COMIRNATY ORIGINAL/OMICRON BA.1,
COMIRNATY ORIGINAL/OMICRON BA.4–5
(COVID-19 mRNA VACCINE)
RISK MANAGEMENT PLAN
Seite 189
Table 74. List of Important Risks and Missing Information
Important identified risks Myocarditis and Pericarditis
Important potential risks None
Missing information Use in pregnancy and while breast feeding
Use in immunocompromised patients
Use in frail patients with co-morbidities (e.g., chronic obstructive
pulmonary disease [COPD], diabetes, chronic neurological disease,
cardiovascular disorders)
Use in patients with autoimmune or inflammatory disorders
Interaction with other vaccines
Long term safety data
https://www.ema.europa.eu/en/documents/rmp-summary/comirnaty-epar-risk-management-plan_en.pdf