Nachdem zuvor schon Anaphylaxie, Parästhesie und Hypoästhesie als Nebenwirkungen benannt wurden, teilt die EMA in ihrem "COVID-19 vaccines safety update" vom 3.8. mit:
»Möglicher Zusammenhang mit Myokarditis und Perikarditis bei Nuvaxovid
Der PRAC ist zu dem Schluss gekommen, dass Myokarditis und Perikarditis nach einer Impfung mit Nuvaxovid auftreten können. Der Ausschuss empfiehlt daher, Myokarditis und Perikarditis als neue Nebenwirkungen in der Produktinformation von Nuvaxovid aufzuführen und eine Warnung auszusprechen, um die Angehörigen der Gesundheitsberufe und die Empfänger des Impfstoffs zu sensibilisieren.
Der Ausschuss hat den Zulassungsinhaber außerdem aufgefordert, zusätzliche Daten über das Risiko des Auftretens dieser Nebenwirkungen vorzulegen. Myokarditis und Perikarditis sind entzündliche Erkrankungen des Herzens. Die Symptome können unterschiedlich sein, umfassen jedoch häufig Atemnot, einen kräftigen Herzschlag, der unregelmäßig sein kann (Herzklopfen), und Schmerzen in der Brust.«
Die Gesamtzahl der Verdachtsfälle wurde seit dem letzten Bericht nicht upgedatet. Mit Stand vom 4.7. werden diese Zahlen berichtet:
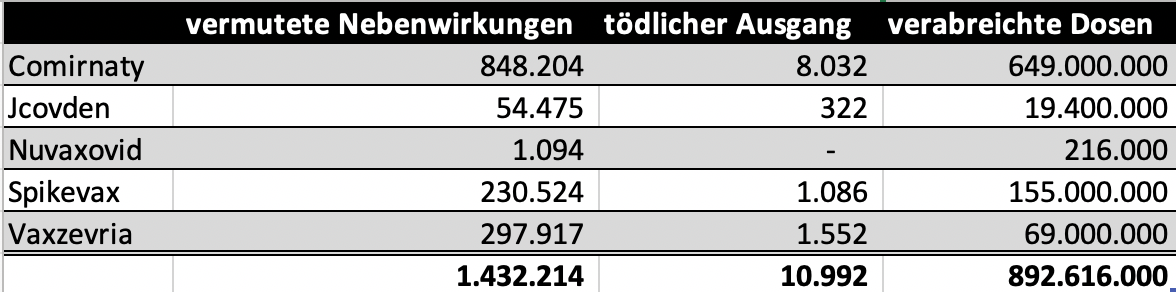
Zum letzten Bericht siehe
EMA: Mehr als 1,4 Millionen Verdachtsfälle. Neue Warnungen zu Novavax, Moderna und Astra Zeneca

Ach, das kleine Risiko nur viermal im Jahr. Für die Förderung der Pharmaindustrie muss man schon ein wenig risikobereit sein. Vielleicht macht Kalle sich ja mal stark für die Einsparung von Papier und schlägt vor, dass die Nebenwirkungen in Schriftgrad 2 gedruckt werden und nur noch jeder "Impfstoffpalette" beigefügt werden müssen. Er kann sich ja mit Gesundheitsschützer Marco B. absprechen.
"Boris entschuldige, dass ich dich störe, gerade habe ich den Lauterbach über sein Infektionsschutzgesetz ab Oktober gehört. Das ist unerträglich und unfassbar. Wer stoppt diesen Voll… (Streichung durch mich, BR)? Ich bin wirklich erschüttert. Warum stoppt den keiner? Entschuldige bitte, du musst mir nichts antworten. Aber ich bin sehr emotional, auch weil ich täglich mitbekomme, dass im Krankenhaus nichts mehr funktioniert":
https://reitschuster.de/post/weniger-als-viermal-geimpften-sollen-faktisch-gekennzeichnet-werden/
@Marc Damlinger: Soll das Journalismus sein?
@aa
Ob das Journalismus ist oder nicht kann und soll jeder selbst entscheiden. Ich bewerte das nicht. Ich nehme es zur Kenntnis und mache mir mein eigenes Bild. Wenn Sie den Artikel gelesen hätten, wüssten Sie, dass diese Zeilen am Ende zu lesen sind und nicht zum Artikel selbst gehören. Diese Zeilen hat Herr Reitschuster bekommen, als er den Artikel geschrieben hat, den ich ober verlinkt hab. Genau das unterscheidet seine Seite von allen anderen, dass er einen ab zu hinter die Kulissen blicken lässt.
@Marc Damlinger: Das ist für mich so transparent wie der anonyme Vater, der für die "Impfung" seines Kindes kämpft. Kann sein, kann nicht sein, ist in beiden Fällen Stimmungsmache.
Die EU Banden, kommen mit über 8 Monatiger Verspärung damit. Gut geschmiert
Donnerstag, 04.08.2022
ld
01.08.22 – Wenn sich nicht einmal die STIKO und der Gesundheitsminister einig sind, dann wird es verwirrend:
Denn in Sachen vierte Corona-Impfung gibt es aktuell Unstimmigkeiten.
Die einen sagen so – die anderen sagen so.
Vielleicht ist auch deshalb die Nachfrage nach dem zweiten Corona-Booster aktuell ziemlich gering
– zumindest im Vogelsbergkreis.
https://osthessen-news.de/n11698015/zweiter-corona-booster-will-die-vierte-impfung-niemand-mehr.html
aus
@tagesthemen
„Der Plan reicht. Das Land befindet sich in einem viel besseren Zustand als noch vor einem Jahr. Viel mehr Menschen sind geimpft." sagt der Bundesjustizminister @MarcoBuschmann
zum neuen #Infektionsschutzgesetz in den #tagesthemen.
Tagesthemen Gespräch mit Bundesjustizminister
6:04 PM · Aug 3, 2022·
https://twitter.com/tagesthemen/status/1554890970742902791
https://twitter.com/jeha2019/status/1554946724166336515
Klaus Stöhr
@stohr_klaus
"Es ist normalerweise unethisch Menschen nicht-getesteten Bekämpf.massnahmen auszusetzen, wenn Studien möglich sind.
Das Umsetzen von Bek.massnahmen,
die keine starke Evidenz haben
verschwendet Resourcen und kann vermeidbaren Schaden verursachen"
https://www.pnas.org/doi/10.1073/pnas.2119887119
One lesson of COVID-19: Conduct more health policy trials | Proceedings of the National Academy of…
One lesson of COVID-19: Conduct more health policy trials
7:37 PM · Aug 3, 2022
https://twitter.com/stohr_klaus/status/1554914460049047552?cxt=HHwWgIC89dGdlZQrAAAA
Wow: 'Damit könnte das Präparat im Idealfall nicht nur vor symptomatischen Erkrankungen schützen, sondern gleich vor einer Infektion.' https://www.faz.net/agenturmeldungen/dpa/bund-foerdert-corona-nasenspray-mit‑1–7‑millionen-euro-18220240.html
https://uncutnews.ch/twitter-zensiert-den-von-pfizerimpfstoff-geschadigten-israelischen-covid-impfstoff-direktor-und-wahrscheinlich-ranghochster-medizinische-wissenschaftler-der-welt/
@Chrissie: Sagt wer? Auf dem üppigen Twitter-Account des Mannes ist das nicht zu lesen (https://twitter.com/shmuelcshapira), wobei ich die hebräischen (?) Tweets nicht verstehe.
Jessica Hamed
@jeha2019
Lieber @Notarzt12
– Ihre Frage ist sehr berechtigt & es wäre vor dem Hintergrund, dass die #einrichtungsbezogeneImpfpflicht mit angeblichem Fremdschutz begründet wird, zwingend, zumindest 20a IfSG anzupassen. Alles andere wäre wegen der fehlenden Kohärenz jur. angreifbar.
Quote Tweet
Notarzt ️
@Notarzt12
· 5h
Frage:
da sich die einrichtungsbezogene Impfpflicht
am Status geimpft orientiert…
wenn nun in den Entwürfen für den Herbst von 3 Monaten die Rede ist…
kann es sein, dass dies dann
auch für die einrichtungsbezogene Impfpflicht gilt?
Alle 3 Monate ?
@aufmerken @jeha2019
7:16 AM · Aug 4, 2022
https://twitter.com/jeha2019/status/1555090366759575552?cxt=HHwWgICxheGc5ZQrAAAA
Klaus Stöhr
@stohr_klaus
·
13m
Der genannte 3‑Monatszeitraum im IfSG-Entwurf vernachlässigt
entweder die Daten zu den Impfzielen oder
den Impfnebenwirkungen.
Impfziel kann es leider nicht sein, Infektionen generell zu verhindern,
sondern die schweren Verläufe bei den Vulnerablen zu minimieren.
https://pbs.twimg.com/media/FZT4C2FXwAIbs7d?format=png&name=small
Quote Tweet
Klaus Stöhr
@stohr_klaus
· 20h
https://n‑tv.de/23503920 Hier meine Beobachtungen.
A. Kommunikationsproblem: Pressemitteilung: unklar welche Masken. FFP2 würde an allen Stellungnahmen der Fachgesellschaften vorbeigehen.
B. Fachl. Grundprobleme:
a. Ein Zeitraum (Okt-April) für Massnahmen egal wie Situation ist.
Show this thread
Klaus Stöhr
@stohr_klaus
·
12m
2. Und wenn man tatsächlich, um die Ausscheidung zu reduzieren, alle 3 Monate Impfungen empfiehlt, hat man noch nichts von den Nebenwirkungen gehört. Besonders evidenzbefreit wird es bei den Genesenen, vor allem wenn sie auch noch geimpft sind. Hier hält der Schutz vor…
Klaus Stöhr
@stohr_klaus
·
12m
3. …schweren Verläufen viel länger an und auch die Ausscheidung ist im Vergleich schwächer.
Besonders makaber erscheint die geplante 3‑Monatsfrist, wenn man sich die Empfehlungen der Stiko hierzu anschaut.
Klaus Stöhr
@stohr_klaus
4. Hier ⬇️wird z.B. eine Auffrischungsimpfung ausschliesslich für Vulnerable nach 2x Impfung und danach Infektion, empfohlen.
https://rki.de/DE/Content/Infekt/EpidBull/Archiv/2022/Ausgaben/21_22.pdf?__blob=publicationFile
https://pbs.twimg.com/media/FZT5KMsXkAAppyn?format=png&name=small
10:41 AM · Aug 4, 2022
https://twitter.com/stohr_klaus/status/1555141862205292547
Mrs M ❤️
@MrsMertes
Wir beobachten eine neue Stufe der Corona-Ausgabe von „Teile und herrsche!“
Sinngemäß: Spalte die Bevölkerung in immer kleinere Gruppen, die sich gegenseitig bekämpfen und Du hast Ruhe.
2021: Geimpfte/Ungeimpfte
NEU-2022: Frischgeimpfte/Altgeimpfte
10:01 AM · Aug 4, 2022
https://twitter.com/MrsMertes/status/1555131692377149442?cxt=HHwWhMC88ZyC-JQrAAAA
Corona Realism Retweeted
Hirnschluckauf
@Hirnschluckauf
Das ist eine FDP2-Maske. Sie dient dazu, den Impfstatus einer Person kenntlich zu machen. Verwendung findet sie ausschließlich in Deutschland.
@fdpbt
@fdp
#FDP2Maske
#Infektionsschutzgesetz
https://pbs.twimg.com/media/FZQju_EXEAAj8zv?format=jpg&name=small
7:08 PM · Aug 3, 2022·Twitter for Android
https://www.bundesgesundheitsministerium.de/fileadmin/Dateien/3_Downloads/Gesetze_und_Verordnungen/GuV/M/MedBVSV.pdf
S.2 ff
".…Weitere Ausnahmen vom Arzneimittelgesetz,
von der Arzneimittel- und Wirkstoffherstellungsverordnung
und der Arzneimittel-Härtefall-Verordnung sowie Anordnung von Maßnahmen
(1) Die nach § 77 AMG zuständige Bundesoberbehörde kann im Einzelfall anordnen, dass abweichend von den
§§ 10 und 11 AMG Arzneimittel ohne eine Kennzeichnung und Packungsbeilage in den Verkehr gebracht werden
dürfen, wenn dies zur Sicherstellung der Versorgung mit Arzneimitteln erforderlich ist. § 11a AMG findet auf diese
Arzneimittel keine Anwendung. Die zuständige Bundesoberbehörde veröffentlicht in diesen Fällen die erforderlichen
Produktinformationen in geeigneter Weise und barrierefrei.
(2) Die nach § 77 AMG zuständige Bundesoberbehörde kann im Einzelfall anordnen, dass abweichend von § 8
Absatz 3 AMG Arzneimittel, deren Verfalldatum abgelaufen ist, in den Verkehr gebracht werden dürfen, wenn dies zur
Sicherstellung der Versorgung erforderlich ist und sie sich davon vergewissert hat, dass die Qualität, Wirksamkeit und
Unbedenklichkeit dieser Arzneimittel nicht wesentlich beeinträchtigt sind.
(3) Die für die Überwachung des Verkehrs mit Arzneimitteln nach § 64 AMG zuständige Behörde kann im Einzelfall
das Inverkehrbringen von Arzneimitteln gestatten, die abweichend von den §§ 13 bis 15 sowie § 19 AMG oder ab-
weichend von den §§ 3, 4, 11, 15, 16 und 17 oder §§ 22 bis 26 der Arzneimittel- und Wirkstoffherstellungsverordnung
(AMWHV) hergestellt wurden, wenn die nach § 77 AMG zuständige Bundesoberbehörde nach Vornahme einer Nutzen-
Risiko-Bewertung feststellt, dass die jeweilige Ausnahme von den genannten Vorschriften zur Sicherstellung der Ver-
sorgung der Bevölkerung mit Arzneimitteln erforderlich ist und die Qualität, Wirksamkeit und Unbedenklichkeit der
herzustellenden Arzneimittel gewährleistet sind.
(4) Die für die Überwachung des Verkehrs mit Arzneimitteln nach § 64 AMG zuständige Behörde kann im Einzelfall
Ausnahmen von den §§ 72, 72a und 73 Absatz 1, 2, 3 und 4 AMG oder § 17 oder § 26 AMWHV gestatten, wenn die
nach § 77 AMG zuständige Bundesoberbehörde nach Vornahme einer Nutzen-Risiko-Bewertung feststellt, dass die
jeweilige Ausnahme von den genannten Vorschriften zur Sicherstellung der Versorgung der Bevölkerung mit Arznei-
mitteln erforderlich ist und die Qualität, Wirksamkeit und Unbedenklichkeit der eingeführten Arzneimittel gewährleistet
sind.
(5) Die nach § 77 AMG zuständige Bundesoberbehörde kann im Einzelfall Ausnahmen von § 21 Absatz 1, den
§§ 22, 24, 25 und 26 Absatz 2, den §§ 28, 29 und 32 AMG zulassen, wenn dies nach Vornahme einer Nutzen-
Risiko-Bewertung zur Sicherstellung der Versorgung der Bevölkerung mit Arzneimitteln erforderlich ist. Abweichend
von § 29 Absatz 2a Satz 3 AMG gilt die Zustimmung zu einer angezeigten Änderung nicht als erteilt, wenn der
Änderung nicht innerhalb einer Frist von drei Monaten widersprochen worden ist.
(6) Die nach § 77 AMG zuständige Bundesoberbehörde kann mit Zustimmung des Bundesministeriums im Einzelfall
Ausnahmen von den im Sechsten Abschnitt des Arzneimittelgesetzes vorgesehenen Fristen auf Basis einer von ihr
durchzuführenden Nutzen-Risiko-Bewertung zulassen, wenn dies zur Sicherstellung der Versorgung der Bevölkerung
mit Arzneimitteln erforderlich ist. Abweichend von § 42 Absatz 2 Satz 4 AMG gilt die Genehmigung einer klinischen
Studie nicht als erteilt, wenn die zuständige Bundesoberbehörde dem Sponsor innerhalb von höchstens 30 Tagen
nach Eingang der Antragsunterlagen keine mit Gründen versehenen Einwände übermittelt.
(7) Die nach § 77 AMG zuständige Bundesoberbehörde kann im Einzelfall abweichend von § 47 Absatz 1 Satz 1
Nummer 2 Buchstabe g AMG gestatten, dass pharmazeutische Unternehmer und Großhändler Arzneimittel, die mit
dem Hinweis „Zur klinischen Prüfung bestimmt“ versehen sind und kostenlos zur Verfügung gestellt werden, an Teil-
nehmerinnen und Teilnehmer einer klinischen Prüfung abgeben dürfen, wenn nach einer von dem Sponsor für den
Einzelfall vorzunehmenden Bewertung die Sicherheit der an der klinischen Prüfung teilnehmenden Personen sowie die
Validität der in der klinischen Prüfung erhobenen Daten gewährleistet sind und die Pseudonymisierung der Prüfungs-
teilnehmerinnen und ‑teilnehmer gegenüber dem Sponsor durch geeignete Maßnahmen sichergestellt ist.
(8) Die nach § 77 AMG zuständige Bundesoberbehörde kann mit Zustimmung des Bundesministeriums im Einzelfall
Ausnahmen von den in § 21 Absatz 2 Nummer 6 AMG und in den §§ 3 und 7 der Arzneimittel-Härtefall-Verordnung
geregelten Voraussetzungen für die Durchführung eines Härtefallprogramms zulassen, sofern dies zur Vorbeugung
und Behandlung von COVID-19 oder von deren Begleiterkrankungen erforderlich ist.
http://www.bundesanzeiger.de
Verkündung
Veröffentlicht am Dienstag, 26. Mai 2020
BAnz AT 26.05.2020 V1
Seite 2 von 4
(9) Die für die Überwachung des Verkehrs mit Arzneimitteln nach § 64 AMG zuständige Behörde kann im Einzelfall
Abweichungen von § 52b Absatz 2 und 3 AMG und den §§ 4, 4a und 6 AM-HandelsV gestatten, wenn die jeweilige
Ausnahme von den genannten Vorschriften zur Sicherstellung der Versorgung der Bevölkerung mit Arzneimitteln er-
forderlich ist.
§ 5
Ausnahmen vom Transfusionsgesetz
Das Paul-Ehrlich-Institut wird ermächtigt, im Einvernehmen mit dem Robert Koch-Institut und mit Zustimmung des
Bundesministeriums angepasst an die vom Deutschen Bundestag nach § 5 Absatz 1 Satz 1 des Infektionsschutz-
gesetzes (IfSG) festgestellte epidemische Lage von nationaler Tragweite
1. abweichend von § 5 Absatz 1 Satz 2 des Transfusionsgesetzes (TFG) und der Richtlinie der Bundesärztekammer
zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie)
gemäß den §§ 12a und 18 des Transfusionsgesetzes vom 4. Oktober 2017 (BAnz AT 06.11.2017 B5) Eignungs‑,
Tauglichkeits- und Rückstellungskriterien für Vollblut, Blutbestandteile und Plasma spendende Personen festzule-
gen, soweit dies unter Abwägung des Nutzen-Risiko-Verhältnisses zur Sicherstellung der Versorgung der Bevölke-
rung mit Blut, Blutbestandteilen und Blutprodukten erforderlich ist,
2. abweichend von den §§ 4 und 7 des TFG und den Vorgaben in der Richtlinie Hämotherapie zur Spendeeinrichtung,
zur Spendeentnahme und zu Laboruntersuchungen vor Spendefreigabe Kriterien festzulegen, soweit dies unter
Abwägung des Nutzen-Risiko-Verhältnisses zur Sicherstellung der Bevölkerung mit Blut, Blutbestandteilen und
Blutprodukten erforderlich ist.
Das Paul-Ehrlich-Institut hat die abweichenden Festlegungen nach den Nummern 1 und 2 barrierefrei auf seiner
Internetseite bekanntzumachen.
§ 6
Ausnahmen von der AMG-Kostenverordnung
Von der Erhebung von Gebühren nach § 1 der AMG-Kostenverordnung für Beratungsgespräche, Verfahren der
Zulassung von Arzneimitteln einschließlich Änderungs- und Verlängerungsverfahren sowie für Genehmigungsverfah-
ren für klinische Prüfungen und für Tätigkeiten im Rahmen der Sammlung und Bewertung von Arzneimittelrisiken wird
abgesehen, sofern Gegenstand des jeweiligen Beratungsgesprächs oder des jeweiligen Verfahrens ein Arzneimittel
zur Behandlung, Vorbeugung oder zur Diagnose von COVID-19 ist.…"
"In Bezug auf die Adipositasbehandlung wurde im Jahre 1998 unter der Federführung von Karl Lauterbach die erste Evidenzbasierte Leitlinie verfasst. Wie viele andere auch war Lauterbach jedoch in keiner Weise inhaltlich an der EBM interessiert. Er nutzt sie vielmehr als Kampfbegriff um Fremdinteressen in der Medizin durchzusetzen. 1998 waren es die der Firma Knoll bzgl. Zulassung des Appetitzüglers Sibutramin mit Empfehlungsgrad 1b. Bei genauer Betrachtung wurde die Literatur höchst einseitig ausgewertet und Warnungen bzgl. Nebenwirkungen dabei unterschlagen. Nach 12 Jahren und etlichen Todesfällen wurde Sibutramin dann endlich vom Markt genommen. Bezüglich Diagnostik und Behandlung von Adipositas repräsentiert diese Leitlinie insgesamt in besonderer Weise den Missbrauch von wissenschaftlicher Schein-Evidenz, um genehme Glaubenssätze „wissenschaftlich“ zu etablieren. Davon profitieren alle möglichen Institutionen, jedoch nicht die betroffenen Patienten."
https://www.achgut.com/artikel/mein_abschied_aus_der_deutschen_gesellschaft_fuer_allgemeinmedizin
Du bist ein Hamster.
Nach dem Impfterror kommt der Nebenwirkungsterror. Menschen sind nur noch x% von irgendwas oder gehören Risikogruppen an. Diese Menschen sind nur noch Komparsen. Für Unternehmer sind sie austauschbar wie eine Handelsware und umso wertvoller je niedriger der Beschaffungspreis.
Die ersten Coronamaßnahmen begannen damit Menschen in die Kurzarbeit, in den Hausarrest und in die Arbeitslosigkeit zu schicken. Gleichzeitig wurde das Sonntagsfahrverbot für LKW ausgesetzt.
Ging es jemals um den Menschen!?